Een nieuwe studie van Wan et al. onderzocht 1.720 melanomen die bij diagnose in een vroeg stadium waren. Aan de hand van 36 klinisch-pathologische kenmerken werd met behulp van ‘machine-learning’-algoritmes voorspeld of en wanneer de tumor zou terugkeren.1 De meest sterke voorspellers bleken de Breslow-tumordikte en de mitotische snelheid.
Nieuwe studieresultaten suggereren dat het grootste deel van de melanoomgerelateerde overlijdens plaatsvindt bij mensen waarbij er een recidief ontstaat van een vroegstadiumtumor (stadium I of II).2 Echter wordt dit recidief pas vaak opgemerkt in de symptomatische gemetastaseerde fase. Om deze reden zou het van sterk toegevoegde waarde zijn om toegang tot prognostische tools te hebben waarmee kan worden bepaald welke patiënten een hoog risico op het ontwikkelen van een recidief hebben.3 Deze patiënten kunnen dan extra worden gemonitord of desgewenst vroegtijdig een behandeling ontvangen.
In de huidige studie van Wan et al. werd een lijst opgesteld van diverse klinisch-pathologische kenmerken die in eerdere literatuur geassocieerd waren met een verhoogd risico op recidief van een eerdere vroegstadiumtumor. Met deze kenmerken werden ‘machine-learning’-modellen ontworpen waarmee aan de hand van kunstmatige intelligentie kon worden voorspeld of en wanneer er een recidief zou ontstaan, aan de hand van de tumorkenmerken.
Totaal werden 1.720 stadium I/II cutane melanomen geïncludeerd, die nog niet waren gerecidiveerd. Hiervan hadden er 1.006 een follow-upperiode van minstens 5 jaar en werden er 930 gematched met melanomen die wel waren gerecidiveerd (n=310). Totaal werden de patiënten voor een mediane periode van 7,2 jaar gevolgd (interkwartielbereik: 3,6-11,6 jaar). In deze tijd recidiveerden 18% van de melanomen, waarvan 48,7% op afstand. De mediane tijd tot het ontstaan van een recidief vanaf de diagnose was 1,9 jaar. De patiënten die een recidief ontwikkelden vertoonden een hoger overlijdensrisico (49% versus 22%; p<0,001).
De melanomen werden gelabeld als gerecidiveerd of niet gerecidiveerd en vijf machine-learning-algoritmes werden ingezet om gerecidiveerde en niet-gerecidiveerde melanomen te classificeren. Met deze modellen werd gekeken naar de recidiefkans op basis van alleen de demografische kenmerken van de patiënt, de recidiefkans op basis van demografische kenmerken plus de medische geschiedenis, en de recidiefkans op basis van de twee voorgaande factoren plus de klinisch-pathologische kenmerken die geassocieerd zijn met recidiefkans.
Bij het gebruik van alleen demografische kenmerken, bleek dat geen van de modellen een acceptabele voorspelling konden maken (externe ‘area under the curve’ [AUC]: <0,65). Na het toevoegen van de medische geschiedenis verbeterden deze AUC-waardes voor de sensitiviteit van het voorspellen (p<0,01), maar niet de positieve voorspellende waarde (p>0,05). Wanneer alle tumorkarakteristieken werden toegevoegd aan de leersets, bleek zowel de AUC als de positieve voorspellende waarde significant te verbeteren voor alle modellen (p<0,001).
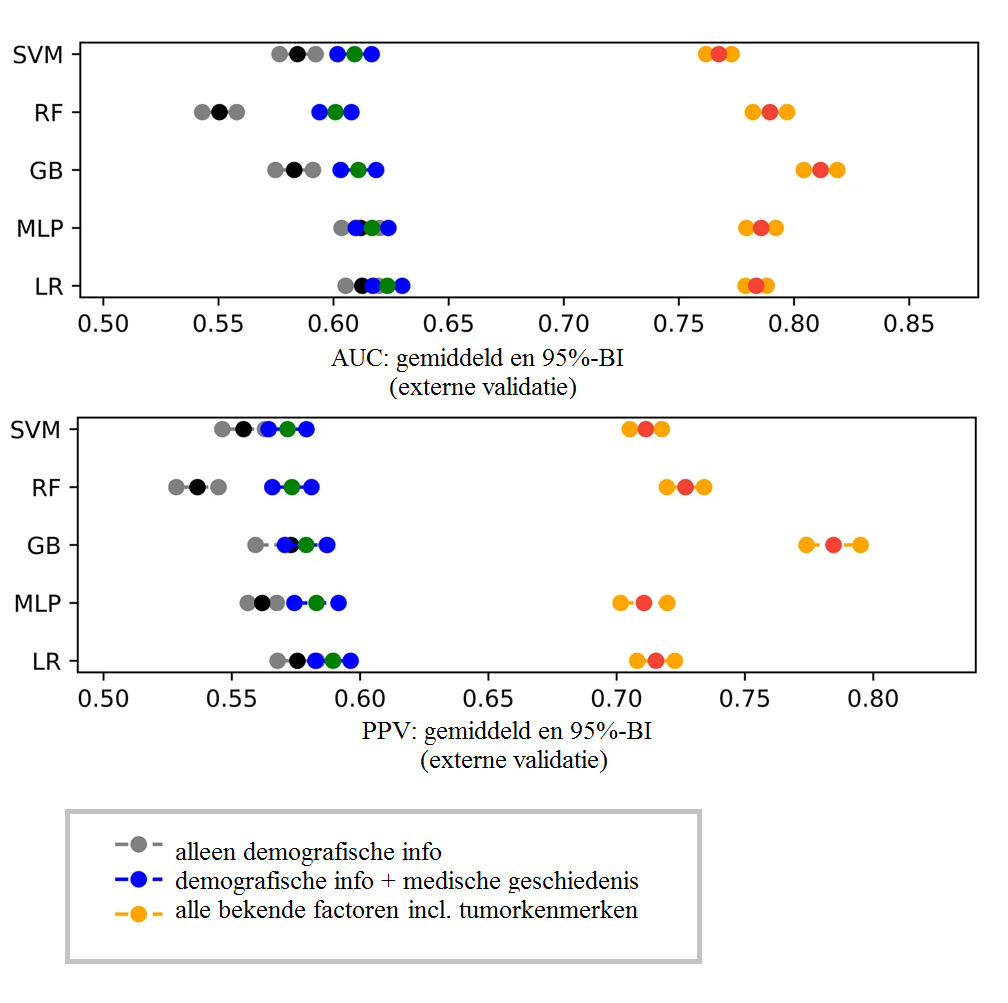
Verder werd onderzocht welke kenmerken de sterkste voorspellende waarde hadden. Dit bleken de Breslow-dikte en de mitotische snelheid te zijn, ook bij diverse subgroepen. Andere voorspellende tumorkenmerken waren onder meer het verzekeringstype, de leeftijd bij diagnose, het mediane inkomen, de tumorplaats en het AJCC-stadium. Verder kon er aan de hand van de modellen een voorspelling worden gemaakt over binnen welke tijdsperiode een recidief zou ontstaan. Hierbij bleken opnieuw de Breslow-tumordikte en de mitotische snelheid de belangrijkste factoren.
In deze nieuwe studie werd gezien dat het mogelijk is om aan de hand van kunstmatige intelligentie met meer dan 80% sensitiviteit te voorspellen welke vroegstadiumtumoren zullen recidiveren. Daarnaast kon er ook een inschatting worden gemaakt op welke termijn dit zou gebeuren. Deze voorspelling werd gemaakt aan de hand van demografische patiëntgegevens, de medische geschiedenis en 36 klinisch-pathologische tumorkenmerken. Aan de hand van deze nieuw ontwikkelde machine-learning-modellen kunnen patiënten worden geïdentificeerd die voordeel kunnen behalen uit additionele monitoring en mogelijk adjuvante immuuntherapie. De onderzoekers suggereren dat het verder verbeteren van de modellen nog mogelijk is, door ook digitale histopathologische afbeeldingen, genoomdata en nieuwe tumorbiomarkers toe te voegen.
Referenties